- 766.00 KB
- 45页
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
清华大学工程热力学课件-第4章(2)
第四章习题课例1(4-7):设有一个能同时产生冷空气和热空气的装置,参数如图所示,判断此装置是否可能?如果不可能,在维持各处原摩尔数和环境t0=0℃不变的情况下,改变哪一个参数就能实现?a2kmol1atm25℃b1kmol1atm1kmol1atm-15℃60℃c
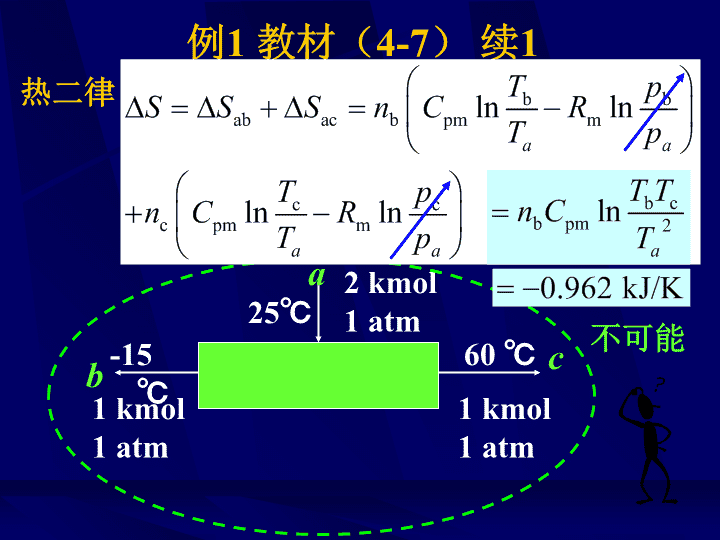
热二律例1教材(4-7)续1a2kmol1atm25℃b1kmol1atm1kmol1atm-15℃60℃c不可能
例1教材(4-7)续2a2kmol1atm25℃b1kmol1atm1kmol1atm-15℃60℃c热一律需向环境放热若吸热,无热源,不可能t0Q
例1教材(4-7)续3a2kmol1atm25℃b1kmol1atm1kmol1atm-15℃60℃ct0Q不可能注意:在使用热二律时,不要忘了热一律!!!
例1教材(4-7)续4例1:(4-7)设有一个能同时产生冷空气和热空气的装置,参数如图所示,判断此装置是否可能?如果不可能,在维持各处原摩尔数和环境t0=0℃不变的情况下,改变哪一个参数就能实现?a2kmol1atm25℃b1kmol1atm1kmol1atm-15℃60℃ct0paTaTcpcTbpb
例1教材(4-7)续5a2kmolpab1kmolpb1kmolpcct0QTaTcTb热一律
例1教材(4-7)续6a2kmolpab1kmolpb1kmolpcct0QTaTcTb热二律
例1教材(4-7)续71)当TaTbTc不变当pb、pc不变,pa当pa不变,pbpc真空不易实现√1)当papbpc不变TbTc不变Ta1.026atm√316.35K43.2℃(25℃)
例2有人声称已设计成功一种热工设备,不消耗外功,可将65℃的热水中的20%提高到95℃,而其余80%的65℃的热水则降到环境温度15℃,分析是否可能?若能实现,则65℃热水变成95℃水的极限比率为多少?已知水的比热容为4.1868kJ/kg.K解:热一律,能量守恒设有1kg65℃的热水0.2kg从65℃提高到95℃,吸热0.8kg从65℃降低到15℃,放热如果吸热量>放热量不满足热一律
例2(续1)0.8kg水从65℃降低到15℃,放热量:0.2kg水从65℃提高到95℃,吸热量:吸热量<放热量可以满足热一律多余热量放给环境,环境吸热量:
例2(续2)Q1环境15℃Q00.2kg从65℃提高到95℃0.8kg从65℃降低到15℃环境吸热热二律取孤立系黑箱法0.2kg6595℃0.8kg6515℃
例2(续3)热二律取孤立系黑箱法0.2kg95℃65℃0.8kg65℃15℃15℃环境吸热可能
例2(续4)有人声称已设计成功一种热工设备,不消耗外功,可将65℃的热水中的20%提高到95℃,而其余80%的65℃的热水则降到环境温度15℃,分析是否可能?若能实现,则65℃热水变成95℃水的极限比率为多少?已知水的比热容为4.1868kJ/kg.K解:热一律,能量守恒令有1kg65℃的热水mkg从65℃提高到95℃,吸热(1-m)kg从65℃降低到15℃,放热
例2(续5)热二律取孤立系黑箱法mkg95℃65℃(1-m)kg65℃15℃15℃环境吸热解得冷热管
关于熵,请你判断下列说法•任何过程,熵只增不减。•若从某一初态经可逆与不可逆两条路径到达同一终点,则不可逆途径的S必大于可逆过程的S。•可逆循环熵变为零,不可逆循环熵变大于零。╳╳╳•不可逆过程S永远大于可逆过程S。╳
请你简答(1)•若工质从同一初态出发,从相同热源吸收相同热量,问可逆与不可逆的末态熵谁大?相同热量,热源T相同>:不可逆过程=:可逆过程相同初态s1相同,
请你简答(2)•若工质从同一初态,分别经可逆和不可逆膨胀过程,到达同一终态,已知两过程热源相同,问传热量是否相同?相同初终态,s相同,>:不可逆过程=:可逆过程热源T相同∴
请你简答(3)•若工质从同一初态出发,一个可逆绝热过程与一个不可逆绝热过程,能否达到相同终点?可逆绝热:不可逆绝热:STp1p2122’
请你简答(4)•理想气体绝热自由膨胀,熵变?典型的不可逆过程AB真空
热二律解决的典型问题2.循环、过程的最大或最小可能性1.循环或过程能否实现可逆时
WhatisEntropy?Entropycanbeviewedasameasureofmoleculardisorder,ormolecularrandomness.Asasystembecomesmoredisordered,thepositionsofthemoleculesbecomelesspredictableandtheentropyincreases.EntropykJ/kg.KGasLiquidSolid
Moleculesinthegasphasepossessaconsiderableamountofkineticenergy.However,weknowthatnomatterhowlargetheirkineticenergiesare,theywillnotrotateapaddlewheelinsertedintothecontainerandproducework.Thisisbecausethegasmolecules,andtheenergytheypossess,aredisorganized.Probablythenumberofmoleculestryingtorotatethewheelinonedirectionatanyinstantisequaltothenumberofmoleculesthataretryingtorotateitintheoppositedirection,causingthewheeltoremainmotionless.Therefore,wecannotextractanyusefulworkdirectlyfromdisorganizedenergy.
Beinganorganizedformofenergy,workisfreeofdisorderorrandomnessandthusfreeofentropy.Thereisnoentropytransferassociatedwithenergytransferaswork.wsh
Thepaddle-wheelworkwillbeconvertedtotheinternalenergyofthegas,asevidencedbyariseingastemperature,creatingahigherlevelofmoleculardisorderinthecontainer.wshGasTOnlyaportionofthisenergycanbeconvertedtoworkbypartiallyreorganizingitthroughtheuseofaheatengine.Therefore,energyisdegradedduringthisprocess,theabilitytodoworkisreduced,moleculardisorderisproduced,entropyisincreased.
Thequantityofenergyisalwayspreservedduringanactualprocess(thefirstlaw),butthequalityisboundtodecrease(thesecondlaw).Thisdecreaseinqualityisalwaysaccompaniedbyanincreaseinentropy.QualityandQuantity
熵的物理意义•可逆过程传热的大小和方向•孤立系熵增(或任何系统的熵产)表征过程不可逆的程度,熵增越大,表明系统不可逆程度越甚。•自然界的过程总是朝着孤立系熵增的方向进行,所以熵可以作为过程方向性的判据。
热力学第二定律的局限性热高温低温,功热,宇宙将失去运动的能量而趋于停息?“热寂说”热二律揭示有限空间中客观现象的规律,不能无限推广!
§4-8Ex及其计算1956,I.郎特(I.Rant)AvailableEnergyEnergyExergy东南大学夏彦儒教授译为如何评价能量的品质???AvailabilityAnergy可用能、有效能可用度火无火用Unavailableenergy无效能
哪个参数才能正确评价能量的价值热量500K293K100kJ1000K100kJ293K
哪个参数才能正确评价能量的价值(续1)焓h1=h2p1p2w1w2w1>w2
哪个参数才能正确评价能量的价值(续2)内能u1=u2p0p0w1w2>
三种不同品质的能量1、可无限转换的能量如:理论上可以完全转换为功的能量高级能量2、不可转换的能量理论上不能转换为功的能量如:环境(大气、海洋)3、可有限转换的能量理论上只能部分转换为功的能量低级能量如:热能、焓、内能(Ex)(An)(Ex+An)机械能、电能、水能、风能
§4-8-1Ex与AnEx的定义当系统由一任意状态可逆地变化到与给定环境相平衡的状态时,理论上可以无限转换为任何其它能量形式的那部分能量,称为Ex100%相互转换功能量中Ex以外的部分就是AnEx即作功能力
Ex——作功能力环境一定,能量中最大可能转换为功的部分500K100kJ1000K100kJT0=293KT0=293K
热一律、热二律与Ex一切过程,Ex+An总量恒定热一律:热二律:可逆过程中,Ex保持不变不可逆过程中,部分Ex退化为AnEx损失、作功能力损失、能量贬值任何一孤立系,Ex只能不变或减少,不能增加——孤立系Ex减原理An不可能转换为ExDegradationofenergy
§4-8-2Ex的计算1、恒温热源T下QExQ:可逆变到环境态时,Q中最大可能转换为功的部分TST0ExQAnQ卡诺循环的功T1.热量的Ex
热量的Ex(续)2、变温热源下的QTST0ExQAnQ微元卡诺循环的功
热量Ex的说明1、Q中最大可能转换为功的部分,就是ExQTST0ExQAnQ2、ExQ=Q-T0S=f(Q,T,T0)Ex损失3、单热源热机不能作功T=T0,ExQ=04、ExQ是过程量T0,Q一定,T一定,QExQEx损失、作功能力损失TExQ
2.冷量的ExT0>T的冷量Q2,有没有Ex卡诺循环的功T0T